- 病毒(virus)
- 最微小的、结构最简单的、专性细胞内寄生的一类非细胞型微生物。
病毒的特点:
- 体积微小(nm 级),可通过细胞滤器,需借助电子显微镜观察
- 遗传物质单一,仅有一种核酸(DNA 或 RNA)
- 严格的活细胞内寄生
- 增殖方式为复制
- 对抗生素不敏感,对干扰素敏感
什么是生命?
- 复制、增殖;
- 进行新陈代谢:
- 获得和利用能量;
- 出生、生长及死亡;
- 应激性:对外界刺激
病毒是介于生命与非生命之间的一种物质形式,既不是生物亦不是非生物。 大多数科学家普遍认为它们是非生命感染颗粒;另外的科学家则表示异议,他们因为病毒在宿主细胞内的活动而认为病毒是活的。
病毒的基本性状
病毒的大小和形态
- 病毒体(virion)
- 有感染性、结构完整、成熟的病毒颗粒。
病毒体积微小,测量单位为 nm,必须借助电子显微镜观察。不同病毒体大小相差很大。
不同病毒的性状不同,多为球型或近似球型,而植物病毒多为杆状。 大多数病毒形状较固定,但有些病毒具有多形性。
病毒的结构
- 核衣壳(capsid)
- 核心(viral core):病毒体的核心部分,主要为核酸,构成病毒基因组(genome),另外还有少量功能性的非结构蛋白。
- 衣壳(capsid):由一定数量的壳粒组成,不同病毒体衣壳所含壳粒数目和排列方式不同,可作为病毒鉴别和分类的依据。
病毒的结构和化学组成
- 包膜(envelope):由某些病毒在成熟过程中以出芽的形式穿过宿主细胞、向外释放过程中获得的宿主细胞的细胞膜或核膜的成分。 根据有无包膜将病毒分为包膜病毒和裸露病毒。
衣壳功能:
- 保护核酸
- 抗原性/免疫原性:诱导机体产生特异性免疫
- 决定病毒对细胞的亲嗜性,介导病毒进入宿主细胞
- 病毒鉴别和分类的依据
衣壳组成:
- 形态亚单位(morphologic subunit):壳粒(capsomere)
- 结构亚单位(structural subunit)/化学亚单位:组成壳粒的多肽分子
根据壳粒排列方式的不同,可将病毒分为三种对称型:
- 螺旋对称型(helical symmetry)
- 20 面体立体对称型(icosahedral symmetry)
- 复合对称型(complex symmetry)
病毒的化学组成和功能
核酸
核酸的功能:
- 病毒复制
- 病毒的遗传信息,决定病毒的遗传特性
- 具有感染性
蛋白质
- 结构蛋白:
- 衣壳蛋白:由多肽亚单位组成,抗原性强
- 包膜蛋白:属糖蛋白
- 基质蛋白:连接衣壳蛋白和包膜蛋白
- 非结构蛋白/功能性蛋白:由病毒的基因组编码,但不参与病毒体构成部分的病毒蛋白多肽
蛋白质的功能:
- 保护病毒核酸
- 参与感染过程
- 具有抗原性
脂质
病毒体的脂类主要存在于包膜中,几乎都是从宿主细胞的细胞膜或核膜上得到的。 可通过脂溶剂去除包膜,使病毒失去感染性。
病毒的增殖
病毒的复制周期
吸附和穿入
吸附
- 吸附(adsorption)
- 病毒体依靠其表面结构与易感细胞膜上特定的病毒受体结合并黏附在细胞膜表面的过程。
- 吸附可分为两个阶段:
- 病毒和细胞的静电结合:非特异性、可逆
- 宿主表面受体与病毒表面结构的特异性结合:特异性、不可逆,是决定病毒感染的真正开始。
穿入
- 穿入(penetration)
- 即细胞进入宿主细胞的过程,主要通过吞饮(endocytosis)、融合(fusion)等方式。
- 吞饮:裸露病毒:病毒与细胞表面结合后内凹入细胞,胞膜内陷形式类似吞噬泡。
- 融合:包膜病毒:病毒包膜与细胞膜密切接触,在融合蛋白的催化下,融合孔开口,病毒包膜与胞膜融合,将病毒的核衣壳释放至细胞内。
脱壳
- 脱壳(uncoating)
- 病毒进入易感细菌脱去蛋白质衣壳的过程。
- 多数病毒在穿入宿主细胞的过程中,靠宿主细胞溶酶体酶的作用使衣壳蛋白水解。
生物合成
- 生物合成(biosynthesis)
- 即病毒利用宿主细胞提供的低分子物质大量合成病毒核酸和结构蛋白。
病毒合成的蛋白质:
- 转录早期 mRNA → 早期蛋白:是在病毒核酸复制之前合成的,主要为用于合成子代 DNA 分子的多种酶类,为功能性蛋白;
- 转录晚期 mRNA → 晚期蛋白:病毒核酸自我复制后,以子代的病毒核酸为模版翻译出来的,主要为构成病毒衣壳的结构蛋白。
病毒核酸的复制方式因核酸类型的不同而异,可分为 7 个类型:双链 DNA 病毒单链 DNA 病毒单正链 RNA 病毒单负链 RNA 病毒双链 RNA 病毒逆(反)转录病毒嗜肝 DNA 病毒
双链 RNA(dsDNA)病毒在细胞核内合成 DNA,细胞质内合成病毒蛋白,痘病毒除外。
单正链 RNA 病毒这类病毒本身就具有 mRNA 的功能。
逆转录病毒核酸以单正链 RNA 形式存在,但不具 mRNA 功能,只能作为逆转录的模版。
组装、成熟、释放
- 组装(ssembly)
- 新合成的子代病毒核酸和蛋白质在宿主细胞内组合成新病毒颗粒的过程。
- 除痘病毒外,DNA 病毒均在细胞核内组装
- RNA 病毒与痘病毒在胞质内组装
释放(release)方式:
- 破胞释放:裸露病毒在宿主细胞内积累到一定数量后,随细胞裂解释放;
- 出芽:包膜病毒在释放过程中包被上了宿主细胞的核膜(疱疹病毒)或细胞膜;
- 通过细胞间桥或细胞融合的方式在细胞间传播,很少释放到细胞外。
病毒的异常增殖与干扰现象
病毒的异常增殖
顿挫感染
- 顿挫感染 | 流产感染(abortive infection)
- 病毒感染宿主细胞后,因细胞不能为病毒提供复制的必要条件(如酶类、能量及必要成分)而没有完整病毒体的产生。
- 非容纳细胞(non-permissive cell):引起病毒顿挫感染的细胞。
- 容纳细胞(permissive cell):能支持病毒完成正常增殖的细胞。
缺陷干扰颗粒
- 缺陷病毒(defective virus)| 缺陷干扰颗粒(defective interfering particle, DIP)
- 因基因组不完整或发生严重改变,而不能复制出完整子代病毒的病毒。
- 缺陷病毒在辅助病毒的帮助下,可以增殖出完整病毒;
- 缺陷干扰颗粒能干扰(属于病毒的 干扰现象)同种成熟病毒体进入细胞。
- 辅助病毒(helper virus)
- 具有弥补缺陷病毒的不足,使之增殖出完整病毒的辅助功能的病毒。
干扰现象
- 干扰现象(interference)
- 两种病毒感染同一细胞时,一种病毒的增殖可以抑制另一种病毒增殖的现象。
干扰现象不仅在活病毒间发生,灭活病毒也能干扰活病毒。
病毒的遗传与变异
遗传型变异
基因突变
- 突变株(mutant)
- 由基因突变产生的病毒表型性状改变的毒株。
- 毒力改变
- 条件致死突变株(conditional lethal mutant):病毒突变后在特定条件下能增殖,在原来的条件下不能增殖而致死的突变株。
- 宿主范围突变株(host-range mutant, hr 突变株):病毒基因组的改变影响了其对宿主细胞的吸附或相互作用。
- 耐药性突变株(drug-resistant mutant)
重组和重配
- 重组(recombination)
- 多种病毒感染同一细胞时,两者发生核酸水平上的交换和重新组合。
- 重配(reassortment)
- 在分节段的 RNA 病毒基因组之间,两个病毒株通过基因节段的交换使子代基因组发生突变的过程。
重组发生在分子内,而重配发生在分子间(每个节段视为一个分子),见下图1:
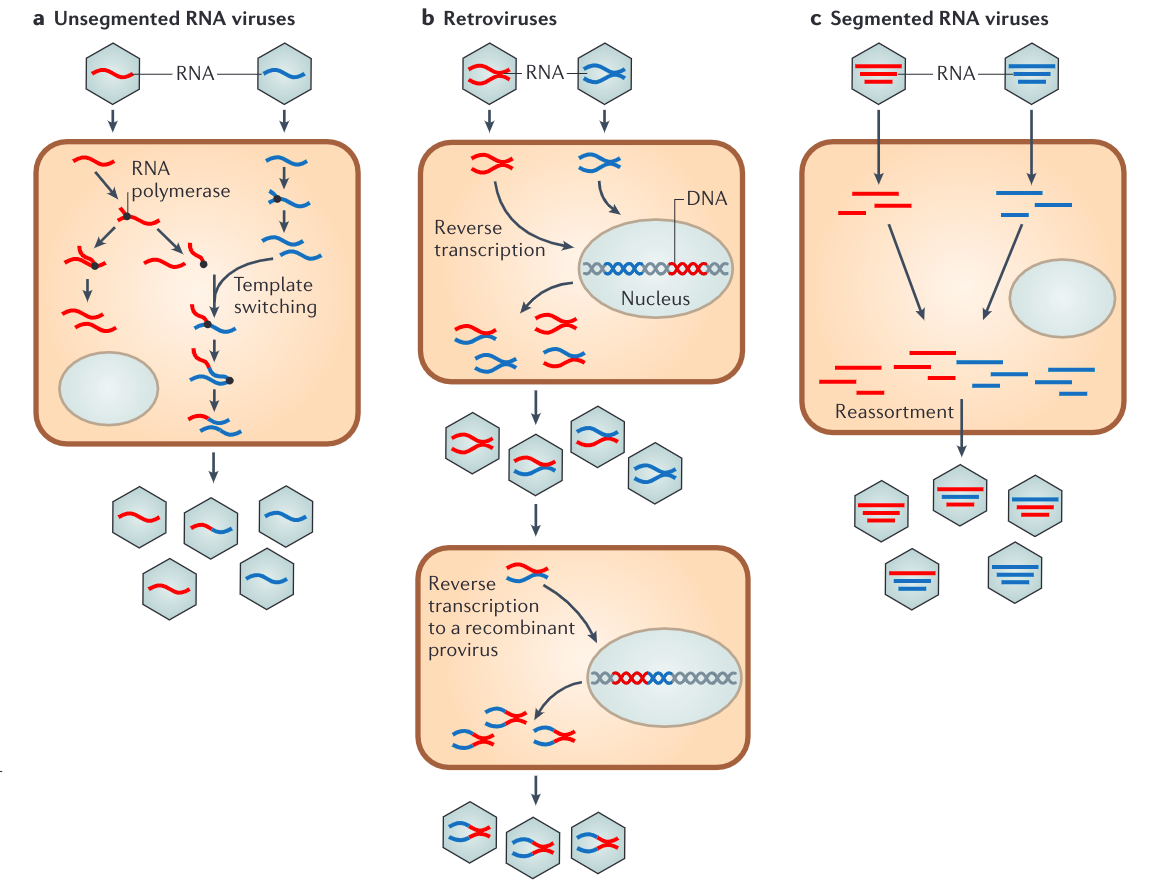
重组和重配
基因整合
- 整合(integration)
- 病毒基因组或基因组中的某些片段插入宿主细胞染色体 DNA 的重组过程。
基因整合可引起病毒基因的变异及宿主细胞染色体基因的改变,导致细胞转化发生肿瘤等。
非遗传性变异
表型混合与核衣壳转移
- 表型混合(phenotypic mixing)
- 一种病毒复制的核酸被另一种病毒编码的蛋白质衣壳或包膜包裹,是基因产物的交换。
- 核衣壳转移(transcapsidation)
- 裸露病毒发生的表型混合。
基因型混合
- 基因型混合(genotype mixing)
- 两种病毒的核酸偶尔混合装在同一个病毒衣壳内,或两种病毒的核衣壳偶尔装在同一个包膜内,
- 核酸未重组,没有遗传性,传代后子代恢复其亲代的性状。
互补
- 互补(complementation)
- 两种病毒通过产生的蛋白质产物互相弥补不足,如辅助病毒和缺损病毒。
增强
- 增强(enhancement)
- 一种病毒对另一种病毒的产量有促进作用。
理化因素对病毒的影响
- 物理因素:温度、PH、射线
- 化学因素:脂溶剂、化学消毒剂、抗生素与中草药、其他(离子等)、脂溶剂(包膜病毒)
病毒的感染与抗病毒免疫
- 病毒感染(viral infection)
- 病毒侵入体内并在靶细胞内增殖,与机体发生相互作用的过程。
- 病毒性疾病(viral disease)
- 病毒感染根据病毒种类、机体状态的不同而产生的轻重不一的损伤。
病毒传播和播散
传播方式:
- 水平传播:经呼吸道、消化道、皮肤(包括虫媒传播)或黏膜、血液、泌尿生殖道传播;
- 垂直传播:母体病原生物经胎盘、产道或乳汁传播给子代,如风疹病毒、巨细胞病毒、乙型肝炎病毒、人类免疫缺陷病病毒等。
病毒在宿主体内的播散方式
- 直接接触播散
- 经血液播散
- 经神经系统播散
病毒的致病机制
病毒感染对宿主细胞的直接作用
- 杀细胞性感染(cytocidal infection)/溶细胞性感染(cytolytic infection):病毒在宿主细胞内复制增殖后,在短时间内释放大量二代病毒,细胞被破坏、死亡,这种作用称为杀细胞效应,这种感染称为杀细胞性感染。
- 稳定状态感染(steady state infection):有些病毒增殖较慢,所致病变较轻;以出芽的方式释放子代病毒,细胞短时间内不会溶解死亡。
- 细胞凋亡(cell apoptosis):由宿主基因控制的细胞程序性死亡,属于正常的生理学现象。
- 病毒基因组的整合(viral integration):病毒的遗传物质结合至宿主细胞的染色体内。
- 细胞增生与细胞转化:
- 细胞增生:少数病毒感染宿主细胞后反而会促进宿主细胞 DNA 的合成。
- 细胞转化(cell transformation):某些病毒感染导致宿主细胞出现形态发生改变、细胞增殖加快、失去细胞间的接触抑制等细胞生物学行为的改变。转化的细胞可能变成肿瘤细胞。
- 包涵体(inclusion body)(衣原体 也能形成包涵体):
- 某些病毒感染细胞后,在细胞浆或/和细胞核内出现的嗜酸性或嗜碱性、大小数量不同的圆形或卵圆形斑块状结构。
- 病毒包涵体是由病毒颗粒和未装配的病毒成分在细胞内堆积而成。
病毒感染的免疫病理作用
- 体液免疫病理作用
- 细胞免疫病理作用
- 病毒感染对免疫系统的致病作用
- 病毒感染引起的自身免疫病
病毒感染类型
隐性感染
- 隐性感染(inapparent infection)| 亚临床感染(subclinical infection)
- 病毒侵入机体后,由于病毒毒力较弱或机体防御力较强,病毒不能大量增殖,对细胞损伤不严重,临床无症状或症状不典型。
显性感染
- 显性感染(apparent infection)
- 病毒侵入后大量增殖致使机体出现典型临床症状。
显性感染包括:
- 急性病毒感染(acute viral infection):潜伏期短,发病急,病程短,恢复后机体不在携带病毒。
- 持续性病毒感染(persistent viral infection):机体可携带潜伏病毒数月至数(十)年;可出现症状,也可不出现症状;引起慢性进行性疾病,并可称为重要的传染源。
- 潜伏(性)感染(latent infection):持续性感染伴有疾病的间歇性发作,在两次发作间用常规方法不能分离到病毒,如 HSV 、水痘-带状疱疹病毒及 CMV 感染(见 人类疱疹病毒)等。
- 慢性感染(chronic infection):持续感染可检出病毒,并常排出病毒,但不发病或带有免疫病理失调,如 HBV 、jc 病毒、BK 病毒、HIV 及 LCMV 感染等。
- 慢发病毒感染(slow virus infection)/迟发(病毒)感染/长程感染:持续感染有很长的潜伏期,随后缓慢的发展成致死性疾病,如 HIV 和痲疹病毒的感染。儿童期感染麻疹病毒恢复后,极少数人于十余年后可发生亚急性硬化性全脑炎(SSPE)。
抗病毒感染免疫
干扰素是机体抗病毒感染免疫的主要细胞因子。
- 干扰素(interferon, IFN)
- 由病毒或其他干扰素诱生剂刺激人或动物细胞产生的一种糖蛋白。
干扰素的作用:
- 广谱抗病毒(无病毒特异性)
- 调节免疫功能
- 抑制肿瘤细胞生长
干扰素不是直接杀伤细胞,而是于宿主细胞的受体结合,进而作用于宿主细胞的基因,使之合成抗病毒蛋白。
干扰素的种类:
- Ⅰ 型干扰素:α 干扰素、β 干扰素
- 由白细胞(α)和成纤维细胞(β)产生
- 抗病毒作用较强
- Ⅱ 型干扰素:γ 干扰素
- 由 T 细胞产生
- 对免疫细胞的调节作用较强
亚病毒
- 亚病毒(subvirus)
- 一些新的非寻常病毒的致病因子,为比病毒更小、结构更简单的微生物。
亚病毒包括类病毒、卫星病毒和朊粒。
- 类病毒(viroid)
- 均为植物病毒,仅由 250~400 个核酸组成,核酸为单链杆状 RNA,有二级结构,无包膜或衣壳,不含蛋白质。
- 类病毒通常通过种子或花粉传播。
- 卫星病毒(satellite virus)
- 一种引起苜蓿(mùxu)绒毛菸(yū)等植物损害的致病因子。分为两大类:
- 可编码自身的衣壳蛋白
- 卫星病毒 RNA 分子,曾称为拟病毒(virusoid),需利用辅助病毒的蛋白质衣壳。
- 朊粒(prion)| 朊病毒 | 传染性蛋白粒子
- 正常宿主细胞基因编码的构象异常的蛋白质,是引起人和动物传染性海绵状脑病的病原体。
- 生物学地位尚未确定,目前归类于亚病毒。
- 抵抗力强:高压蒸气灭菌(134℃,2h)
- 所致疾病:
- 动物海绵状脑病:羊瘙痒病牛海绵状脑病(疯牛病)
- 人海绵状脑病:库鲁病克雅病克雅病变种(主要通过消化道感染)
Simon-Loriere, E., Holmes, E. Why do RNA viruses recombine?. Nat Rev Microbiol 9, 617–626 (2011). https://doi.org/10.1038/nrmicro2614 ↩︎