人体肌组织可分为骨骼肌、心肌、平滑肌三类,前两者在光学显微镜下显现明暗交替的横纹,故统称为横纹肌。骨骼肌受躯体运动神经的支配和控制,称随意肌;心肌和平滑肌受自主神经的调控称非随意肌。
横纹肌
骨骼肌神经-肌接头处的兴奋传递
- 骨骼肌神经-肌接头(neuromuscular junction)
- 运动神经末梢与其所支配的骨骼肌细胞之间的特化结构,由接头前膜、接头后膜和接头间隙构成。
骨骼肌神经-肌接头的结构
- 接头前膜(prejunctional membrane)
- 运动神经轴突末梢膜的一部分
- 接头前膜内侧的轴浆中含约 3×105 个突触囊泡(synaptic vesicle)或突触小泡,每个囊泡内含约 104 个乙酰胆碱(acetylcholine,ACh)分子。
- 接头间隙(junctional cleft)
- 接头前膜与接头后膜之间 20–30 nm 的间隔,充满细胞外液。
- 接头后膜(postjunctional membrane)| 终板膜(end-plate membrane)
- 与接头前膜相对的骨骼肌细胞膜,呈向内凹陷的浅槽。
- 接头后膜上含有 N2 型 ACh 受体阳离子通道(N2-ACh receptor cation channel),集中分布于皱褶的开口处。
- 在接头后膜外表面还分布有乙酰胆碱酯酶(acetylcholinesterase),它能将 ACh 分解为胆碱和乙酸。
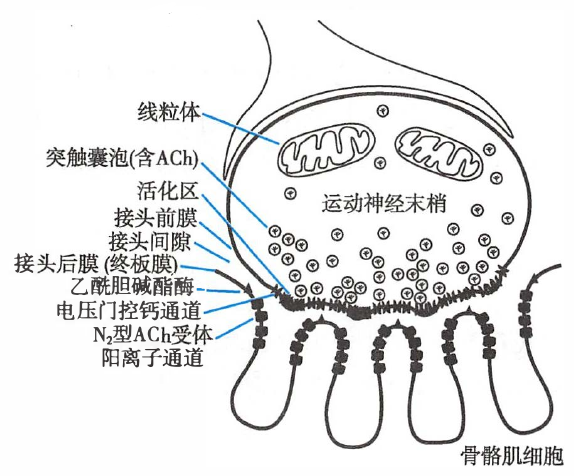
骨骼肌神经-肌接头的结构
骨骼肌神经-肌接头兴奋传递过程
骨骼肌神经-肌接头兴奋传递过程
N2 型 ACh 受体阳离子通道,可允许 Na+,K+ 和 Ca2+ 跨膜移动,但主要是 Na+ 内流和 K+ 外流;在静息状态下,Na+ 内向驱动力大于 K+ 外向驱动力1,故以 Na+ 内流为主。
终板电位
- 终板电位(end-plate potential,EPP)
- 属于局部电位,幅度可达 50–75 mV,不会出现反极化,可以电紧张方式向周围扩布,刺激邻近的普通肌膜(非终板膜)中的电压门控钠通道开放,引起 Na+ 内流和普通肌膜的去极化,当去极化达到阙电位水平时即可爆发动作电位。
- 微终板电位(miniature end-plate potential,MEPP)
- 在静息状态下,因囊泡的随机运动也会发生单个囊泡的自发释放,并引起终板膜电位的微弱去极化,称作微终板电位。
- 接头前膜一次兴奋产生的 EPP 是由大量囊泡同步释放所引起的 MEPP 发生总和而形成的。
- 属于局部电位,具有相应的特点。
- 终板膜上没有电压门控钠通道,不产生动作电位,但可通过电紧张传播的方式刺激周围肌膜中的电压门控钠通道开放,产生动作电位。
- 在 ACh 释放后几毫秒内,ACh 即被终板膜外侧的乙酰胆碱酯酶迅速分解而消除其作用,使终板膜恢复到接受新兴奋传递的状态。
影响骨骼肌神经-肌接头兴奋传递的因素
- 作用于 N2 型 ACh 受体阳离子通道:
- 筒箭毒碱、α-银环蛇毒:特异性阻断终板膜中的 N2 型 ACh 受体阳离子通道,松弛肌肉
- 自身抗体:破坏 N2 型 ACh 受体阳离子通道,可导致重症肌无力
- 作用于乙酰胆碱酯酶
- 新斯的明:抑制乙酰胆碱酯酶,改善肌无力患者的症状
- 有机磷农药:磷酸化胆碱酯酶,使其丧失活性而引起中毒症状
- 除极化型肌松药/非竞争型肌松药,如琥珀胆碱(司可林),分子结构与 ACh 相似并有相同活性,与神经肌肉接头后膜上的胆碱受体有较强亲和力,且不易被胆碱酯酶水解,在与胆碱受体结合后产生持续的高局部电位,使得电压门控 Na+ 通道在第一次去极化激活后保持失活状态而不能回到静息状态。
- 使用性增强现象:强直后增强:反复的刺激导致突触前膜 Ca2+ 的蓄积,导致随后的刺激引起囊泡释放的增加。
横纹肌细胞的结构特征
横纹肌细胞的结构特征是细胞内含有大量的肌原纤维和高度发达的肌管系统。
肌原纤维和肌节
横纹肌细胞内含有上千条直径 1–2 μm、纵向平行排列的肌原纤维,由粗、细肌丝构成。由于粗、细肌丝在肌节中的规则排列,肌原纤维在光镜下沿长轴可见明暗交替的横纹,分别称为明带和暗带。
明带中只有细肌丝,而暗带中有粗肌丝,因而表现出透光度的差异。暗带中,H 带以外的部分为粗、细肌丝的重叠部分,而 H 带只有粗肌丝。
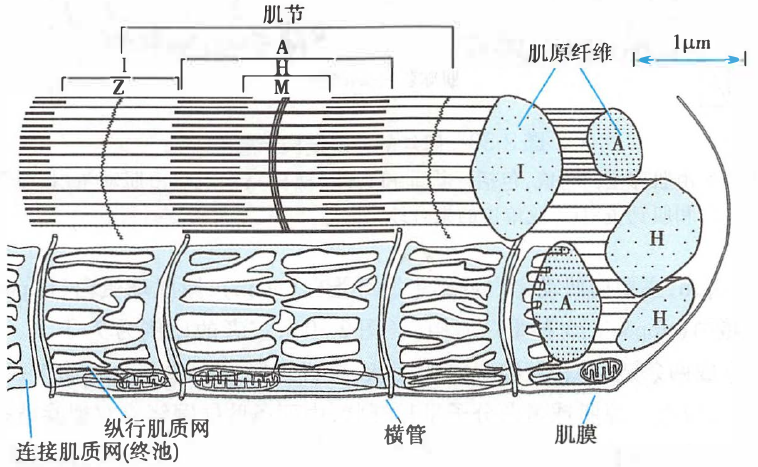
骨骼肌的肌原纤维和肌管系统
A:暗带(粗肌丝全长);H:暗带中的 H 带;M:暗带中的 M 线;
I:明带(细肌丝不与粗肌丝重合的长度);Z:明带中、分隔肌节的 Z 线(Z 盘)
相邻两 Z 线之间的区段称为肌节(sarcomere),是肌肉收缩和舒张的基本单位。
肌管系统
横纹肌细胞中有横管和纵管两种肌管系统。
- 横管/T 管(T tubule,transverse tubule):与肌原纤维走行方向垂直的膜性管道,由横纹肌细胞膜内陷并向深部延伸而成,可将沿肌膜传导的电信号迅速传至肌原纤维。
- 纵管/L 管(L tubule,longitudinal tubule)/肌质网(sarcoplasmic reticulum,SR):与肌原纤维走行方向平行的膜性管道。
- 回收 Ca2+:纵行肌质网(longitudinal SR,LSR):在肌原纤维周围包绕、交织成网的肌质网,其膜上有钙泵,可逆浓度梯度将胞质中 Ca2+ 转运至 SR 内,从而中止横桥周期。
- 释放 Ca2+:连接肌质网(junctional SR,JSR)/终池(terminal cisterna):SR 与 T 管膜或肌膜(见于心肌)相接触的、膨大或呈扁平状的末端,其内的 Ca2+ 浓度约比胞质中高近万倍。
JSR 膜中嵌有钙释放通道(calcium release channel)或称雷诺丁受体(ryanodine receptor,RYR),其分布与 T 管膜或肌膜上的 L 型钙通道(L-type calcium channel)相对应。
在骨骼肌,T 管与其两侧的终池形成三联管(triad)结构;在心肌,T 管与单侧的终池相接触形成二联管(diad)结构,都是兴奋-收缩耦联的关键部位。
横纹肌细胞的收缩机制肌丝滑行理论
横纹肌的收缩机制一般用肌丝滑行理论(myofilament sliding theory)来解释,即横纹肌的肌原纤维由与其走向平行的粗肌丝和细肌丝构成,肌肉的缩短和伸长系粗肌丝与细肌丝在肌节内发生相互滑行所致,而粗肌丝和细肌丝本身的长度均不改变。
依据:在光镜下观察到,横纹肌收缩时肌肉缩短,暗带(粗肌丝)宽度不变,只有明带和 H 带(非粗、细肌丝重叠部分)相应变窄。
肌丝的分子结构
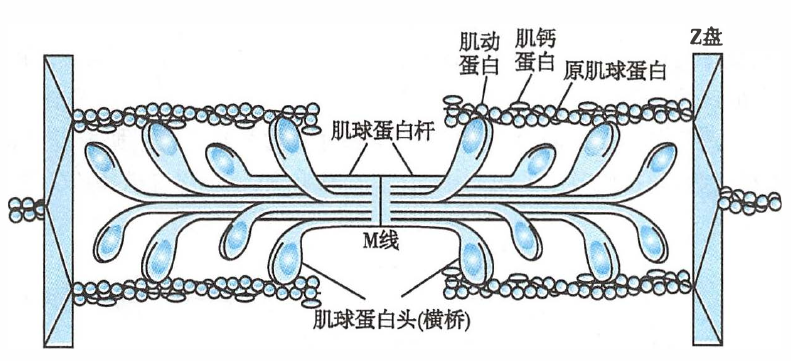
肌丝的分子结构
- 粗肌丝:主要由数百个肌球蛋白(或称肌凝蛋白,myosin)分子聚合而成,单个肌球蛋白分子呈豆芽状,有一个杆部和两个球形的头部,由 6 条肽链构成。
- 细肌丝:主要由肌动蛋白(或称肌纤蛋白,actin)、原肌球蛋白(tropomyosin,或称原肌凝蛋白)和肌钙蛋白(troponin)3 种蛋白质构成,三者的比例为 7:1:1。
- 肌动蛋白:单体为球形分子,通过聚合成两条链,并相互缠绕成双螺旋状,构成细肌丝的主干。肌动蛋白分子上有多个粗肌丝横桥结合位点。
- 原肌球蛋白:呈长杆状,多个原肌球蛋白分子首尾相接,形成长链,长度为肌动蛋白中连续 7 个单体的总长度,沿肌动蛋白双螺旋的浅沟旁走行,阻止横桥与肌纤蛋白(肌动蛋白)结合。
- 肌钙蛋白:由肌钙蛋白 T(troponin T,TnT)、肌钙蛋白I(troponin I,TnI)和肌钙蛋白 C(troponin C,TnC)3 个亚单位构成,以一定的间距(7 个肌动蛋白单体的长度)出现在原肌球蛋白的双螺旋结构上。
Ca2+ 结合肌钙蛋白,拉开原肌球蛋白,暴露肌动蛋白的横桥结合位点,横桥(肌球蛋白)与之结合并发生构象变化,引发肌丝滑行。
奇怪的名字:肌球蛋白不是球状,肌动蛋白不主动运动
- 横桥(cross-bridge)
- 由粗肌丝头部连同与它相连的一小段称为“桥臂”的杆状部从肌丝中向外伸出而形成的结构。
- 横桥具有 ATP 酶活性,并能与肌动蛋白结合。横桥被激活后可向 M 线方向扭动,成为肌丝滑行的动力来源。
肌球蛋白和肌动蛋白直接参与肌肉收缩,故称为收缩蛋白(contractile protein);而原肌球蛋白和肌钙蛋白不直接参与肌肉收缩,但可调控收缩蛋白间的相互作用,故称为调节蛋白(regulatory protein)。
肌丝滑行的过程横桥周期
粗肌丝与细肌丝间的相互滑行,是通过横桥周期(cross-bridge cycling)完成的。横桥周期是指肌球蛋白的横桥与肌动蛋白结合、扭动、复位的过程。
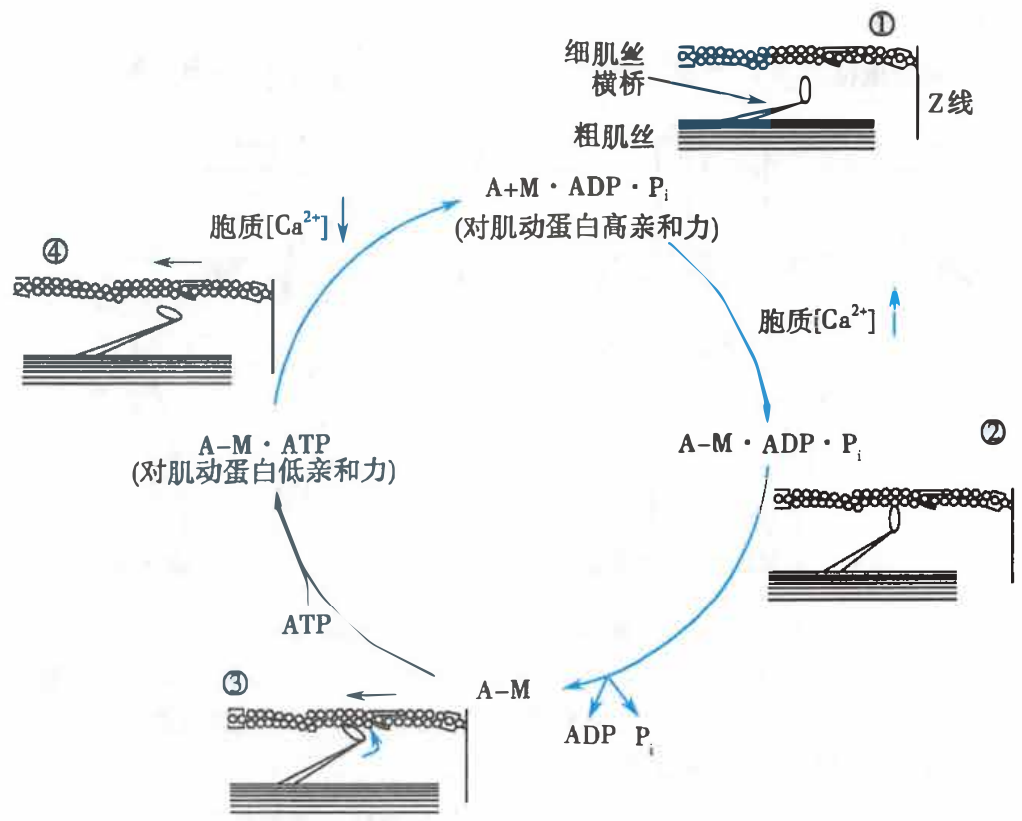
横桥周期
A:肌动蛋白;M:肌球蛋白;A-M:肌动蛋白与肌球蛋白结合物
- 在舒张状态下,横桥的 ATP 酶活性分解与之结合的 ATP 产生能量使上次扭动过的横桥复位,横桥同时与 ADP 和磷酸结合而处于高势能和高亲和力状态;
- 胞质中浓度升高的 Ca2+(通过肌钙蛋白以及原肌球蛋白)触发横桥与肌动蛋白结合;
- 横桥构象改变使其头部向桥臂方向扭动 45°,产生“棘齿作用”(ratchet action)而拖动细肌丝向 M 线方向滑行,横桥储存的势能被用来克服负荷的张力和(或)缩短肌节长度(能量转换),同时与横桥结合的 ADP 和无机磷酸被解离;
- 横桥再与 ATP 结合导致亲和力降低而与肌动蛋白分离,重复上述过程。
一个横桥周期所需时间为 20–200 毫秒,其中横桥与肌动蛋白结合的时间约占一半。若胞质中的 Ca2+ 浓度降低(纵行肌质网回收 Ca2+)则横桥周期停止。
横纹肌细胞的兴奋-收缩耦联
- 兴奋-收缩耦联(excitation-contraction coupling)
- 将横纹肌细胞产生动作电位的电兴奋过程与肌丝滑行的机械收缩联系起来的中介机制。
- T 管膜的动作电位传导:肌膜上的动作电位沿 T 管(横管)膜传至肌细胞内部,并激活 T 管膜和肌膜中的 L 型钙通道。
- JSR 内 Ca2+ 的释放:肌膜的去极化,在骨骼肌可通过构象变化触发钙释放机制,在心肌则通过钙诱导钙释放机制,使 JSR 内的 Ca2+ 顺浓度差释放到胞质中,胞质内的 Ca2+ 浓度由静息时的 0.1 μmol/L 水平迅速升高百倍以上。
- Ca2+ 触发肌丝滑行:胞质内 Ca2+ 浓度的升高促使 Ca2+ 与 TnC 结合而触发肌肉收缩。见横桥周期。
- JSR(实际是 LSR)回摄 Ca2+:
- 在骨骼肌,胞质内增加的 Ca2+ 几乎全部经激活 LSR 膜中的钙泵而被回摄进 SR 中;
- 而心肌胞质内的 Ca2+ 大部分经 LSR 膜中的钙泵活动被回收,尚有 10%–20% 的 Ca2+ 则由肌膜中的 Na+-Ca2+ 交换体和钙泵排至胞外。 胞质中 Ca2+ 浓度降低则导致肌肉舒张,可见肌肉舒张的过程亦耗能。
心肌细胞由于只有单侧的终池(二联管),导致终池释放的 Ca2+ 仅占胞质 Ca2+ 增量的 80%–90%,还有部分来自胞外,同时,兴奋-收缩耦联后,也只有 80%–90% 被回收到 LSR 中。
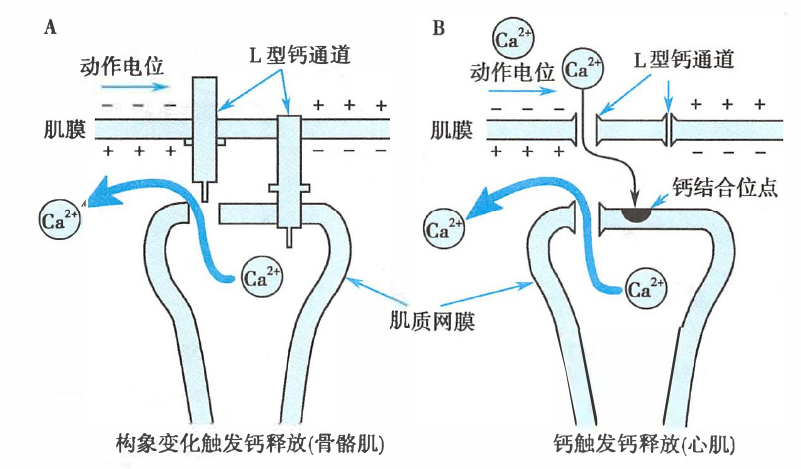
横纹肌肌质网钙离子释放机制
- 骨骼肌:肌膜去极化 → L 型钙通道发生“拔塞”样构象变化 → 肌质网网上的钙释放通道开放
- 心肌:肌膜去极化 → 激活 L 型钙通道 → 使少量 Ca2+ 内流 → Ca2+ 与肌质网膜中的钙结合位点 → 钙释放通道开放
影响横纹肌收缩效能的因素
肌肉收缩可分为等长收缩和等张收缩。
影响横纹肌收缩效能[肌肉收缩时产生的张力大小、缩短程度(幅度),以及产生张力或缩短的速度]的因素包括前负荷、后负荷、肌肉收缩能力及收缩的总和等。
前负荷
- 前负荷(preload)
- 肌肉在收缩(包括等长收缩)前所承受的负荷。
- 由于前负荷即为牵拉肌肉的力量,前负荷越大肌肉就被拉得越长,因而前负荷决定肌肉在收缩前的长度,即初长度(initial length),此时因肌肉受到牵拉而弹性回位的张力属于被动张力。
在等长收缩实验中,可测定不同初长度条件下肌肉主动收缩产生的张力(即主动张力),对应作图即得到长度-张力关系曲线(length-tension relationship curve)。
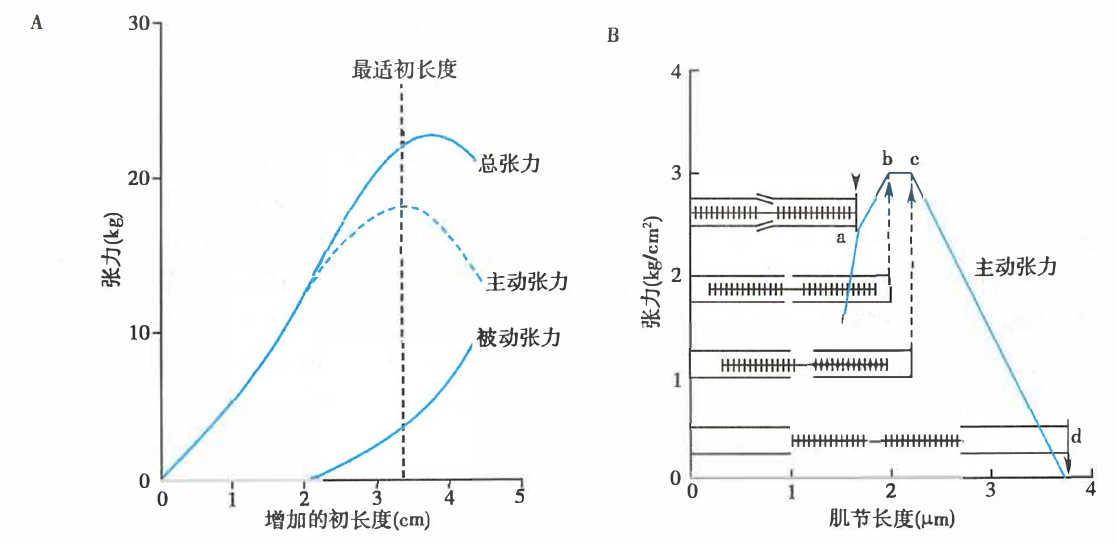
肌肉等长收缩时的长度-张力关系
A. 长度-张力关系曲线,主动张力=总张力-被动张力;B. 肌节的长度-张力关系示意图
可以看出,存在一个最适初长度,此时不仅全部横桥都能发挥作用,而且肌丝间的相互关系也最适合于横桥的活动,使肌肉能产生最大收缩(主动)张力。与最适初长度相对应的肌节长度为 2.0–2.2 μm。适当增加肌肉前负荷,可以增加肌肉的主动张力。
骨骼肌的最适初长度即为一般静息状态下的长度,而心肌的最适初长度则接近舒张期储备用尽时的长度。
后负荷
- 后负荷(afterload)
- 肌肉在收缩后所承受的负荷。
- 由于肌肉在等张收缩时产生的收缩张力与后负荷大小相等,方向相反,故在数值上可用后负荷反映收缩张力的大小。
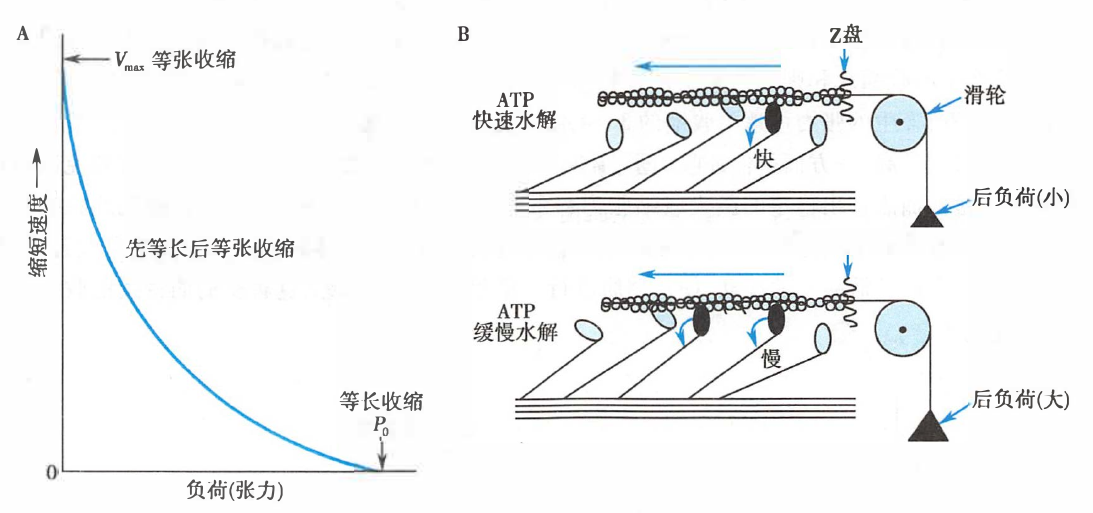
肌肉等张收缩时的速度-张力关系
A. 张力-速度关系曲线;B. 负荷对横桥周期的影响
后负荷增大时,肌肉产生的张力增大,而缩短的速度减慢(可能是由于非结合状态、可活动的横桥减少),肌肉等张收缩的时间缩短,收缩距离也缩短。关于横桥周期,后负荷增大时,横桥摆动速度减慢[这也巧妙地使更多的横桥同时处于与肌动蛋白结合的状态(图中黑色横桥)以维持张力],横桥周期延长。
肌肉收缩能力
- 肌肉收缩能力(contractility)
- 与前负荷和后负荷无关,又能影响肌肉收缩效能的肌肉内在特性。
- 兴奋-收缩耦联过程中胞质内 Ca2+ 浓度的变化、与肌丝滑行有关的横桥 ATP 酶活性、肌细胞能量代谢水平、各种功能蛋白及其亚型的表达水平以及肌原纤维的肥大与否(心肌肥大会使需氧量增加,易发生心绞痛)等。
- 机体的神经和体液调节系统、一些致病因素和治疗药物也可通过影响这些内在特性,调节肌肉收缩能力,这在心肌要比在骨骼肌具有更重要的生理意义。
甲状腺激素可增强肌肉收缩能力
甲状腺激素可以增加几乎所有 ATP 酶的活性:
- Na+-K+ 泵活性:氧化磷酸化↑,小肠吸收葡萄糖↑
- Ca2+ 泵
- 横桥 ATP 酶:肌肉收缩能力增强
- 增加进入细胞的 Ca2+
- 连续的动作电位,使 Ca2+ 通道连续开放
- 增加单次动作电位进入细胞的 Ca2+
- 增加对 Ca2+ 的敏感性
收缩的总和
多纤维总和空间总和多运动单位总和
- 多纤维总和(multiple fiber summation)
- 原指多根肌纤维同步收缩产生的叠加效应。
- 在整体情况下,骨骼肌都以一个运动神经元及其轴突分支所支配的全部肌纤维所构成的运动单位(motor unit)为基本单位进行收缩,其叠加效应通常是参与同步收缩运动单位数目的增加,故又称为多运动单位总和。
频率总和时间总和
- 频率总和(frequency summation)
- 指提高骨骼肌收缩频率而产生的叠加效应,这是运动神经元通过改变冲动发放频率调节骨骼肌收缩形式和效能的一种方式。
- 单收缩(twitch)
- 当动作电位频率很低时,每次动作电位之后出现一次完整的收缩和舒张过程,这种收缩形式称为单收缩。
- 复合收缩
- 由于(骨骼肌)完成一次收缩过程需要的时间远长于动作电位的时间,故动作电位频率增加到一定程度时,后一动作电位所触发的收缩就可叠加于前一次收缩,产生收缩的总和。
- 不完全强直收缩(incomplete tetanus)
- 后一次收缩过程叠加在前一次收缩过程的舒张期,所产生的收缩总和。
- 完全强直收缩(complete tetanus)
- 后一次收缩过程叠加在前一次收缩过程的收缩期,所产生的收缩总和。两次阈刺激之间的间隔小于收缩期。
- 生理情况的骨骼肌收缩几乎均属于完全强直收缩。
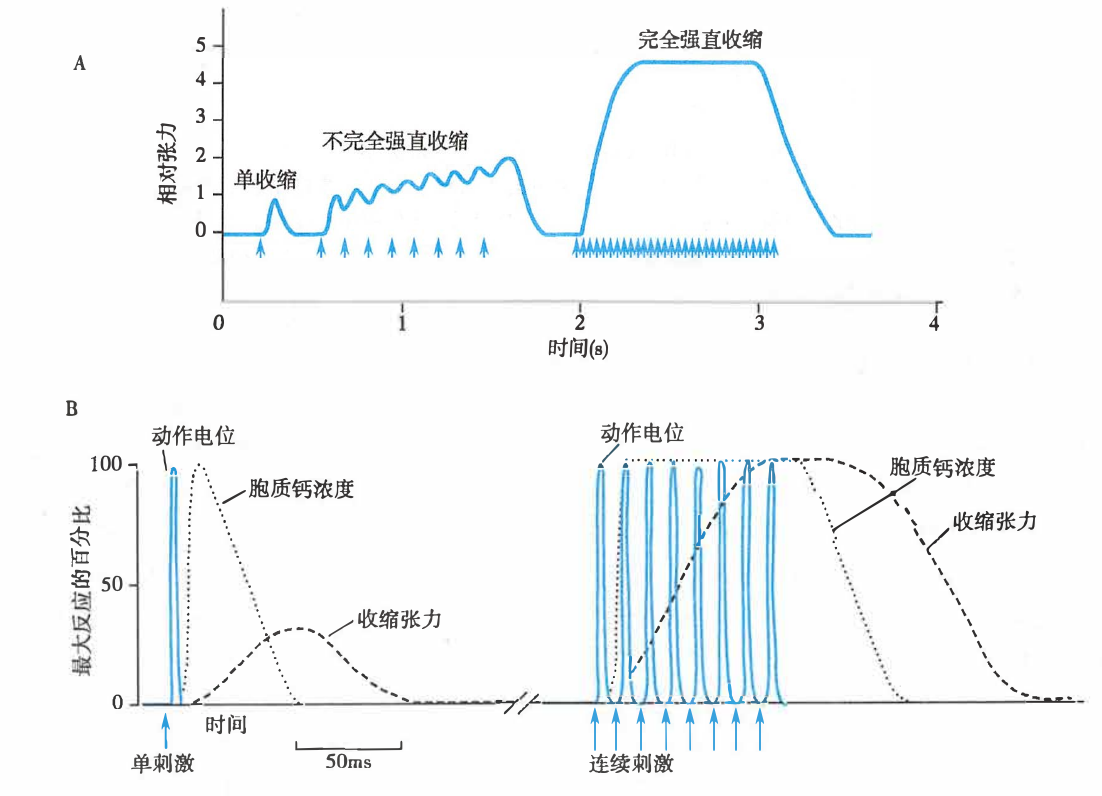
刺激频率对骨骼肌收缩形式(A)和胞质钙浓度(B)的影响
强直收缩时,肌细胞连续兴奋,使胞质 Ca2+ 浓度持续升高,肌张力增大。
- 肌紧张
- 在静息状态下,运动神经也经常发放较低频率的冲动,使骨骼肌进行一定程度的强直收缩,这种微弱而持续的收缩即为肌紧张。
9 版《生理学》表 2-1,32 ↩︎